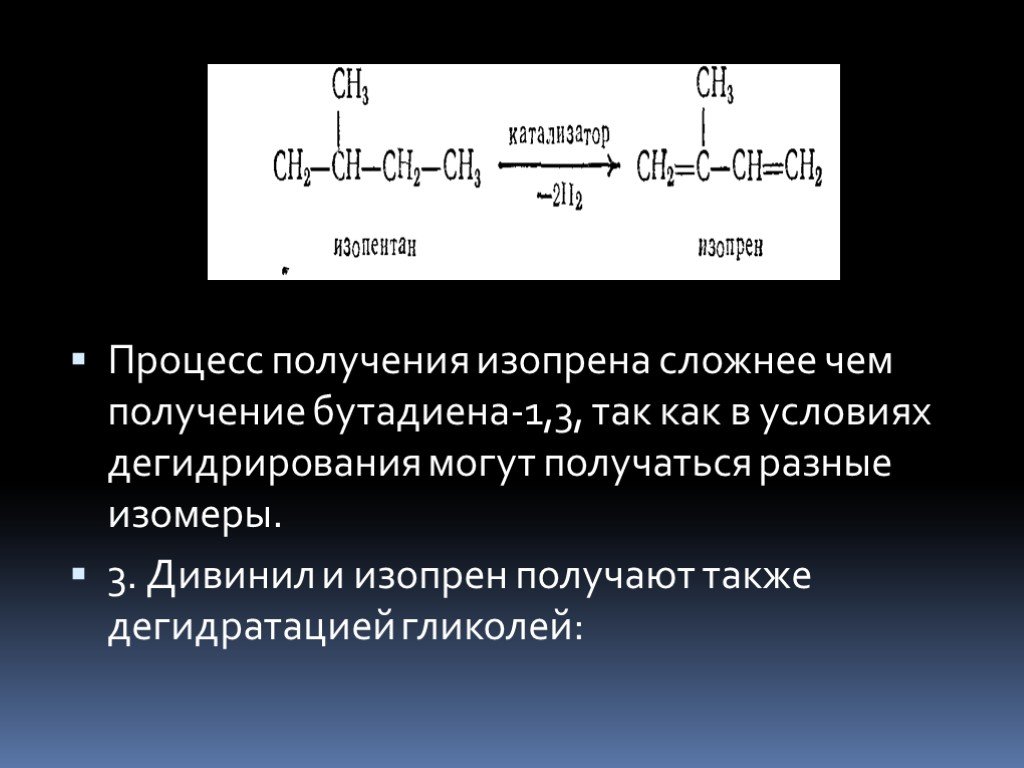
Изопрен получение: ХиМиК.ru — Изопрен
Содержание
Изопрен | это… Что такое Изопрен?
Изопрен СН2=С(СН3)-СН=СН2, 2-метилбутадиен-1,3 — ненасыщенный углеводород диенового ряда (CnH2n−2). В нормальных условиях бесцветная жидкость. Он является мономером для натурального каучука и структурной единицей для множества молекул других природных соединений — изопреноидов, или терпеноидов. [1]. Растворим в спирте. Изопрен полимеризуется, давая изопреновые каучуки. Изопрен также вступает в реакцию полимеризации с соединениями винилового ряда.
Содержание
|
Нахождение и получение
Натуральный каучук является полимером изопрена — наиболее часто цис-1,4-полиизопреном с молекулярной массой от 100,000 до 1,000,000. В качестве примесей содержит несколько процентов других материалов, таких как белки, жирные кислоты, смолы и неорганические вещества. Некоторые источники натурального каучука называются гуттаперча и состоит из транс-1,4-полиизопрена, структурный изомер, который имеет схожие, но не идентичные свойства.[2] Изопрен производится и выделяется в атмосферу многими видами деревьев (главный из них — дуб) Годовое производство изопрена растительностью около 600 млн т., причем половина производится тропическими широколистными деревьями, остальное производится кустарниками.[3] После попадания в атмосферу изопрен превращается свободными радикалами (такими как гидроксил (OH) радикал) и в меньшей мере озоном [4] в различные вещества, такие как альдегиды, гидроксипероксиды, органические нитраты и эпоксиды, которые смешиваются с водными каплями, образуя аэрозоли или дымку.[5][6] Этот механизм деревья используют не только для того, чтобы избежать перегрева листьев Солнцем, но и для защиты от свободных радикалов, особенно озона.
В качестве примесей содержит несколько процентов других материалов, таких как белки, жирные кислоты, смолы и неорганические вещества. Некоторые источники натурального каучука называются гуттаперча и состоит из транс-1,4-полиизопрена, структурный изомер, который имеет схожие, но не идентичные свойства.[2] Изопрен производится и выделяется в атмосферу многими видами деревьев (главный из них — дуб) Годовое производство изопрена растительностью около 600 млн т., причем половина производится тропическими широколистными деревьями, остальное производится кустарниками.[3] После попадания в атмосферу изопрен превращается свободными радикалами (такими как гидроксил (OH) радикал) и в меньшей мере озоном [4] в различные вещества, такие как альдегиды, гидроксипероксиды, органические нитраты и эпоксиды, которые смешиваются с водными каплями, образуя аэрозоли или дымку.[5][6] Этот механизм деревья используют не только для того, чтобы избежать перегрева листьев Солнцем, но и для защиты от свободных радикалов, особенно озона. [7] Изопрен впервые был получен термической обработкой натурального каучука.[8] Наиболее промышленно доступен как продукт термического крекинга лигроина или масла, а также как побочный продукт при производстве этилена. Производится около 20,000 тонн в год. Около 95% производства изопрена используется для производства цис-1,4-полиизопрена — синтетического варианта природного каучука.
[7] Изопрен впервые был получен термической обработкой натурального каучука.[8] Наиболее промышленно доступен как продукт термического крекинга лигроина или масла, а также как побочный продукт при производстве этилена. Производится около 20,000 тонн в год. Около 95% производства изопрена используется для производства цис-1,4-полиизопрена — синтетического варианта природного каучука.
Биологическая роль
В основном, изопрен наиболее часто встречающийся углеводород находящийся в теле человека. Оценочная скорость производства изопрена в теле человека 0.15 мк моль/кг/ч, эквивалентно приблизительно 17 мг для человека весом 70 кг. Изопрен также встречается в низких концентрациях во многих видах пищи.
Изопрен производится в хлоропластах листков обычных видов деревьев через en:DMAPP процесс. Энзим изопрен синтаза ответственна за его биосинтез. Изопрен накапливается и помогает стабилизировать мембраны клеток в ответ на термический стресс, давая некоторую толерантность к термическим ожогам. Изопрен может также давать некоторую устойчивость к реактивным кислородным веществам. Количество изопрена выделенного из изопрен испускающих растений зависит от массы листьев, их площади, света и температуры листьев. Так, в течение ночи, немного изопрена выделяется из листьев дерева, тогда как днём эмиссия существенна (~5-20 мг/м²/ч) в жаркий и солнечный день.
Изопрен может также давать некоторую устойчивость к реактивным кислородным веществам. Количество изопрена выделенного из изопрен испускающих растений зависит от массы листьев, их площади, света и температуры листьев. Так, в течение ночи, немного изопрена выделяется из листьев дерева, тогда как днём эмиссия существенна (~5-20 мг/м²/ч) в жаркий и солнечный день.
Изопрен основной структурный мотив в биологических системах. Терпены (например, каротины являются тетратерпенами) происходят из изопрена, также как терпеноиды и кофермент Q. Также производными изопрена являются: фитол, ретинол(витамин А),токоферол (Витамин E),en:dolichol и en:squalene. Гем имеет изотерпеноидный хвост и ланостерол, и стерол — прекурсор в животных, происходящий из en:squalene и следовательно из изопрена. Функциональная изопреновая единца в биологических системах это диметилаллил фосфат (ДМАФФ) и его изомер изопентенил пирофосфат (ИПФ), которые используется в биосинтезе терпенов и производных ланостерола.
Фактически все организмы производные изопрена синтезируют в en:HMG-CoA reductase pathway. Добавление этих цепочек к протеинам называется en:isoprenylation
Добавление этих цепочек к протеинам называется en:isoprenylation
Биосинтез и его ингибирование статинами
Ингибиторы HMG-CoA редуктазы, также известные как группа холестерол-понижающие препараты называемые статинами, ингибируют синтез мевалоновой кислоты. Мевалонат является прекурсором к en:isopentenyl pyrophosphate, который соединяясь с его изомером en:dimethylallyl pyrophosphate в повторяющемся чередовании образует изопреновую (полипрениловую) цепь.
Статины понижают концентрацию холестерола, который синтезирован из 15-углеродного изотерпеноида en:farnesyl pyrophosphate, также ингибируют все другие изопрены, включая кофермент Q10. Это flow chart показывает биосинтез изопренов, и точку при которой статины действуют ингибируя этот процесс.
Получение
Метод Лебедева:
2Ch4-Ch3-OH -> Ch3=CH-CH=Ch3 + 2h3O + h3 (при t= 425гр., с AL2O3 и ZNO)
Способ дегидрирования двухстадийное каталитическое дегидрирование н-бутана Ch4-Ch3-Ch3-Ch4 -> Ch3=CH-CH=Ch3 + 2h3
получение изопрена из 2-метилбутана
h4C-CH(Ch4)-Ch3-Ch4-->(t=600)h3C=C(Ch4)-CH=Ch3+h3 2-метилбутан изопрен
Дивинил и изопрен в небольших количествах так же выделяют из продуктов пиролиза нефти.
Применение
Изопрен применяют для получения синтетического каучука.
Ссылки
- ↑ NIKLITSCHEK, M.; JENNIFER ALCAÍNO , SALVADOR BARAHONA , DIONISIA SEPÚLVEDA, CARLA LOZANO, MARISELA CARMONA, ANDRÉS MARCOLETA, CLAUDIO MARTÍNEZ2, PATRICIA LODATO, MARCELO BAEZA, and VÍCTOR CIFUENTES (2008). «Genomic organization of the structural genes controlling the astaxanthin biosynthesis pathway of Xanthophyllomyces dendrorhous».
- ↑ Hans Martin Weitz and Eckhard Loser «Isoprene» in Ullmann’s Encyclopedia of Industrial Chemistry 2002, Wiley-VCH, Weinheim. DOI:10.1002/14356007.a14_627
- ↑ Guenther, A.; T. Karl, P. Harley, C. Wiedinmyer, P. I. Palmer and C. Geron (2006). «Estimates of global terrestrial isoprene emissions using MEGAN (Model of Emissions of Gases and Aerosols from Nature)». Atmos. Chem. Phys. 6: 3181–3210.
- ↑ IUPAC Subcommittee on Gas Kinetic Data Evaluation — Data Sheet Ox_VOC7, 2007|url= http://www.

- ↑ Organic Carbon Compounds Emitted By Trees Affect Air Quality, ScienceDaily, Aug. 7, 2009|url=http://www.sciencedaily.com/releases/2009/08/090806141518.htm
- ↑ A source of haze, ScienceNews, August 6th, 2009|url=http://www.sciencenews.org/view/generic/id/46200/title/A_source_of_haze
- ↑ Sharkey, TD; AE Wiberley, and AR Donohue (2007). «Isoprene Emission from Plants: Why and How». Annals of Botany 101 (1): 5–18. DOI:10.1093/aob/mcm240. PMID 17921528.
- ↑ C. G. Williams, Proceedings of the Royal Society 1860 10.
См. также
- Полиизопрен
Изопреновый каучук — виды, характеристики, свойства
31.10.2020
// Каучуки
Содержание статьи:
- Формула изопренового каучука
- Получение изопренового каучука
- Применение изопренового каучука
- Вулканизация изопренового каучука
- Свойства изопренового каучука
Изопреновый каучук – это форма природного каучука, но в модифицированной и адаптированной химическим образом вещество.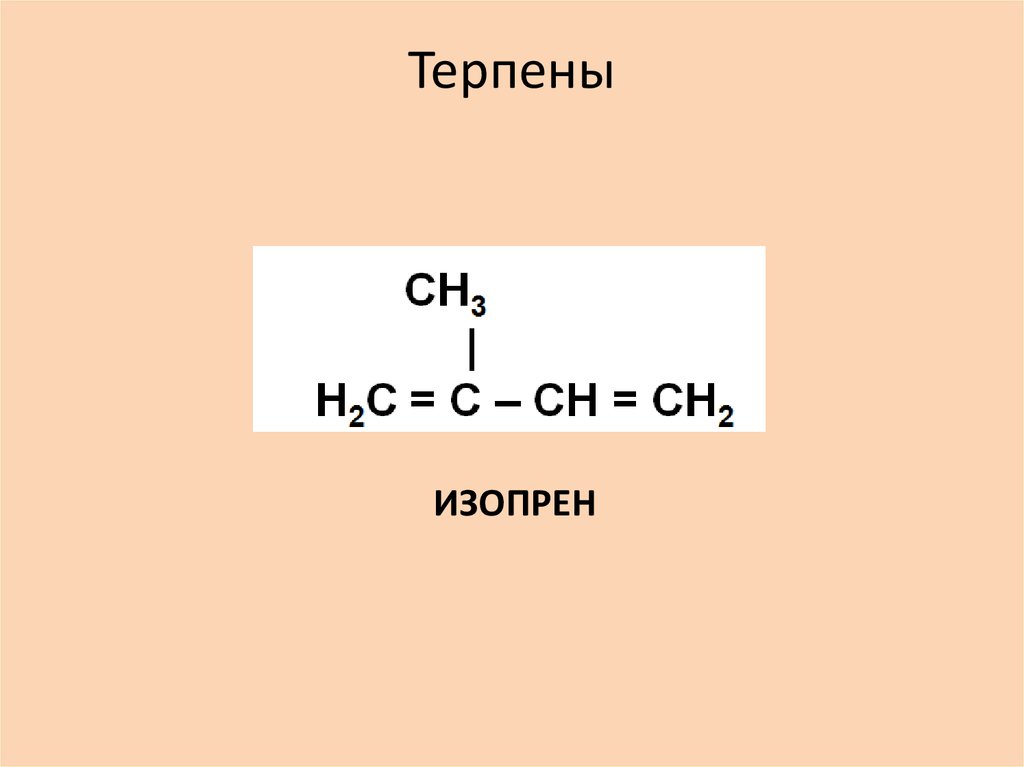
Формула изопренового каучука
nСН2=С(СН3)-СН=СН2 → (-СН2-С(СН3)=СН-СН2-)n
Данный вид каучука очень похож на природный и представляет собой серую массу синтетического вещества без запаха. Его производят путем всевозможных химических процессов. Натуральный каучук – это и есть изопреновый каучук. Поэтому ученым нужно было придумать как разработать эту сложную, но при этом простую формулу.
Синтез изопренового каучука удался, но не в полной мере как у натурального. У него строение групп СН расположены не беспорядочно, как в искусственном, а находятся по одну сторону двойной связи в каждом звене. Иными словами, получить эту связь искусственным путем просто невозможно. Этот факт еще раз доказывает уникальность природы и всех веществ, которые она производит.
Иными словами, получить эту связь искусственным путем просто невозможно. Этот факт еще раз доказывает уникальность природы и всех веществ, которые она производит.
Для справки – природный каучук получают из дерева, именуемым Гевея. Нашли его на берегах Южной Америке. В других растениях есть подобные составы, но они менее качественные, нежели чем в дереве. Натуральный каучук белого цвета, которое после добычи меняет цвет до коричневого или черного. Молочко добывают из дерева, путем надрезания его коры. Подробнее
Природный каучук при нагревании и замерзании резко меняют свои свойства, поэтому ученые придумали методы, которые делали вещество твердым и при этом пластичным, и эластичным, т.е. с сохранением всех необходимых свойств. Один из таких процессов называется вулканизацией. Речь о нем будет ниже.
Получение изопренового каучука
В основе данного соединения лежит особое вещество, именуемое изопреном. Оно представляет собой бесцветный газ, который практически не растворяется в воде, но хорошо взаимодействует со спиртом, бензолом, этанолом.
После того как была выполнена процедура полимеризации для предотвращения окисления его стабилизируют при помощи фенил диамина. Вводят его в жидком виде, чаще всего в формате жидкости. Для того чтобы получить изопреновый каучук, как осадок в виде специфических мелких частичек, полученное вещество смешивают с паром, потом вводят специальные добавки, которые предотвращают создание комочков. После данных манипуляций производят отделение крошки от воды и специальную сушку. После сушки процедуру по созданию изопренового каучука можно считать завершенным.
Применение бутадиен-стирольного каучука
Так как у природного каучука высокие свойства прочности и при этом эластичности, учёные стремились повторить эту формулу.
· Производство шин для автомобилей, мотоциклов и самолётов.
· Различные детали для разного рода промышленных изделий, машин и профессионального и бытового оборудования.
· Транспортерные ленты больших размеров и образцов для крупных производств.
· В медицинских целях для создания деталей или изделий потиру одноразовых и многоразовых перчаток.
· Производство изделий резиновых для мебельных фурнитур.
· Заводы по изготовлению резиновых изделий: игрушки, посуда, кухонная утварь, в том числе.
· Производство презервативов.
· Производство кабелей и разного рода проводов активно использует изопреновый каучук, потому что он обладает высокой степенью изолирования от электричества.
· В производстве прорезиненных поверхностей, ковриков и иных изделий, имеющие резиновые детали.
Вулканизация изопренового каучука
Вулканизация – это технологический процесс, на основании которого происходит соединение некоторых исходных веществ, с целью получения единого соединения, обладающего необходимыми качествами. В частности, речь идет про изопреновый каучук. Данная процедура происходит с участием серы в основе своей и других соединений и нагревании их до определенной температуры.
Вулканизация позволяет насыщаться резине серой и становиться более упругой и прочной. Изготовленная резина из каучука, прошедшего вулканизацию способна сохранять свои свойства под влиянием высоких температур и быть более стойкими к воздействиям различного рода воздействиям окружающей среды. Однако, если серы будет больше положенного, то такой каучук напротив становится боле хрупким и теряет свои эластичные свойства. В этой связи получают новое вещество, именуемое эбонитом.
Современные технологии не стоят на месте и вулканизацию производят не только с добавлением серы, хоть она приоритетней. Существуют способы добавлять в каучук мел или сажу, что значительно снижает стоимость получаемого вещества, потому что сфера применения и использования высокая. Чаще всего подобные составы используются для производства недорогих резиновых изделий или расходников.
Стоит заметить, что природный каучук тоже используется производствами. Чаще всего для создания покрышек для автомобилей. Но данное использование приходится лишь частично. Происходит смешивание натурального с синтетическим, потому что спрос очень высок на подобные прочные и качественные резиновые соединения.
Таким образом, изопреновый каучук – это приближенный вид каучука к природному. Обладает отличными свойствами по прочности, эластичности и высокой электроизоляции, что позволяет применять данный состав в широкой сфере промышленного и бытового назначения, в том числе пищевой, медицинской и автомобилестроительной. Практически ни один вид производства не обходится без участия изопренового каучука в той или иной мере.
Практически ни один вид производства не обходится без участия изопренового каучука в той или иной мере.
Свойства бутадиен-стирольного каучука
Данный каучук имеет следующие свойства:
· Замерзает при охлаждении и кристаллизуется.
· Хорошая эластичность.
· Прочность и истирание на высоком уровне, собственно, как и у всех каучуков
· Вязкий, что и придает ему тягучесть и прочность.
· Плохая стойкость к солнечному свету и высоким температурам.
· Обладает плохой клейкостью с другими веществами.
Каучук обладает хорошей пластичностью. Это значит, что ему можно придать любую форму при необходимости. Помимо этого, он не растворяется в воде и спирту. Возможно набухание с себе подобными веществами — бензин, керосин. При охлаждении каучука до -70 он приобретает некоторые свойства стекла: является хрупким, твердым и гладким, его с легкостью можно расколоть на мелке осколки. Как и все каучуки изопренов преобладает в трёх основных состояниях — вязком, тяжело тягучем и твёрдо-хрупком.
Как и все каучуки изопренов преобладает в трёх основных состояниях — вязком, тяжело тягучем и твёрдо-хрупком.
Стоить заметить, что химическая промышленность потому и синтезирует каучуки разного вида, чтобы он имел каждый раз свойства, подходящие под определенные задачи. Изопреновый каучук прочен и позволяет изготавливать из него резиновые детали, в том числе шины для авиационных и автомобильных производств.
Производство изопрена, одного из прекурсоров топлива высокой плотности, из скорлупы арахиса с использованием высокоэффективного метода предварительной обработки для удаления лигнина
1. Матос С.Т., Гувейя Л., Мораис А.Р. Производство изопрена микроводорослями и бактериями. Зеленый хим. 2013;15(10):2854–2864. doi: 10.1039/C3GC40997J. [CrossRef] [Google Scholar]
2. Линдберг П., Парк С.А. Разработка платформы для фотосинтетического производства изопрена цианобактериями с использованием Synechocystis в качестве модельного организма. Метаб Инж. 2010;12(1):70. doi: 10.1016/j.ymben.2009.10.001. [PubMed] [CrossRef] [Google Scholar]
Метаб Инж. 2010;12(1):70. doi: 10.1016/j.ymben.2009.10.001. [PubMed] [CrossRef] [Google Scholar]
3. Чандра Р., Такеучи Х., Хасегава Т. Производство метана из лигноцеллюлозных отходов сельскохозяйственных культур: обзор в контексте второго поколения производства биотоплива. Renew Sustain Energy Rev. 2012;16(3):1462–1476. doi: 10.1016/j.rser.2011.11.035. [CrossRef] [Google Scholar]
4. Найк С.Н., Гоуд В.В., Раут П.К., Далай А.К. Производство биотоплива первого и второго поколения: всесторонний обзор. Renew Sustain Energy Rev. 2010;14(2):578–597. doi: 10.1016/j.rser.2009.10.003. [CrossRef] [Google Scholar]
5. Hong IK, Jeon H, Lee SB. Сравнение красных, бурых и зеленых водорослей по процессу ферментативного осахаривания. J Ind Eng Chem. 2014;20(5):2687–2691. doi: 10.1016/j.jiec.2013.10.056. [CrossRef] [Google Scholar]
6. де Фигейредо Ф.К., Карвалью А.Ф.А., Бриенцо М., Кампиони Т.С., де Олива-Нето П. Снижение химических затрат при щелочной экстракции арабиноксилана и лигноцеллюлозы и производстве ксилоолигосахаридов. Биоресурсная технология. 2017; 228:164–170. doi: 10.1016/j.biortech.2016.12.097. [PubMed] [CrossRef] [Google Scholar]
Биоресурсная технология. 2017; 228:164–170. doi: 10.1016/j.biortech.2016.12.097. [PubMed] [CrossRef] [Google Scholar]
7. Wang S, Li R, Yi X, Fang T, Yang J, Bae HJ. Производство изопрена на ферментативном гидролизате скорлупы арахиса с использованием различных методов предварительной обработки. Биомед Рез Инт. 2016;2016:1–8. [Бесплатная статья PMC] [PubMed] [Google Scholar]
8. Стефановски Б., Керлинг С., Ормондройд Г. Оценка лигноцеллюлозных ореховых отходов как абсорбента газообразного формальдегида. Ind Crops Prod. 2017;98:25–28. doi: 10.1016/j.indcrop.2017.01.012. [Перекрестная ссылка] [Академия Google]
9. Бентли Ф.К., Мелис А. Диффузионный процесс поглощения углекислого газа и выделения изопрена в газообразных/водных двухфазных фотобиореакторах фотосинтетическими микроорганизмами. Биотехнология Биоинж. 2012;109(1):100–109. doi: 10.1002/bit.23298. [PubMed] [CrossRef] [Google Scholar]
10. Harvey BG. Топливо высокой плотности из изопрена. Патент США 9650314 B1, 2016.
11. Gomaa L, Loscar ME, Zein HS, Abdel-Ghaffar N, Abdelhadi AA, Abdelaal AS, Abdallah NA. Повышение продукции изопрена за счет гетерологичной экспрессии гена изопренсинтазы Кудзу (kIspS) в Bacillus spp. клеточный завод. Амб Экспресс. 2017;7(1):161. doi: 10.1186/s13568-017-0461-7. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
12. Micali E, Chehade KA, Isaacs RJ, Andres DA, Spielmann HP. Распознавание изопреноидного субстрата белковой фарнезилтрансферазой зависит от двойных связей изопрена и разветвленных метильных групп. Биохимия. 2001;40(41):12254–12265. doi: 10.1021/bi011133f. [PubMed] [CrossRef] [Google Scholar]
13. Meylemans HA, Quintana RL, Harvey BG. Эффективное преобразование чистого и смешанного терпенового сырья в топливо высокой плотности. Топливо. 2012;97: 560–568. doi: 10.1016/j.fuel.2012.01.062. [CrossRef] [Google Scholar]
14. Санадзе Г. Природа газообразных веществ из листьев Robinia pseudoacacia . Респ. Академия Наук ГрузССР. 1957;19(8):3. [Google Scholar]
Академия Наук ГрузССР. 1957;19(8):3. [Google Scholar]
15. Sharkey TD, Wiberley AE, Donohue AR. Эмиссия изопрена растениями: почему и как. Энн Бот. 2007;101(1):5–18. doi: 10.1093/aob/mcm240. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
16. Мелис А. Эффективность преобразования солнечной энергии в фотосинтезе: минимизация хлорофилловых антенн для максимальной эффективности. Растениевод. 2009 г.;177(4):272–280. doi: 10.1016/j.plantsci.2009.06.005. [CrossRef] [Google Scholar]
17. Yang J, Zhao G, Sun Y, Zheng Y, Jiang X, Liu W, Xian M. Производство биоизопрена с использованием экзогенного пути MVA и изопренсинтазы в Escherichia coli . Биоресурсная технология. 2012; 104: 642–647. doi: 10.1016/j.biortech.2011.10.042. [PubMed] [CrossRef] [Google Scholar]
18. Кларк Дж. Х., Луке Р., Матару А.С. Зеленая химия, биотопливо и биопереработка. Энн Рев Хим Биомол Инж. 2012;3(1):183. doi: 10.1146/annurev-chembioeng-062011-081014. [PubMed] [CrossRef] [Академия Google]
19. Wagner WP, Nemecek-Marshall M, Fall R. Три различные фазы образования изопрена во время роста и спорообразования Bacillus subtilis . J Бактериол. 1999;181(15):4700–4703. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Wagner WP, Nemecek-Marshall M, Fall R. Три различные фазы образования изопрена во время роста и спорообразования Bacillus subtilis . J Бактериол. 1999;181(15):4700–4703. [Бесплатная статья PMC] [PubMed] [Google Scholar]
20. Хонг С.Ю., Цурбригген А., Мелис А. Производство изопреновых углеводородов при гетерологичной трансформации Saccharomyces cerevisiae . J Appl Microbiol. 2012;113(1):52–65. doi: 10.1111/j.1365-2672.2012.05319.x. [PubMed] [CrossRef] [Академия Google]
21. Yang J, Xian M, Su S, Zhao G, Nie Q, Jiang X, Zheng Y, Liu W. Увеличение производства биоизопрена с использованием гибридного пути MVA и изопренсинтазы в E. coli . ПЛОС ОДИН. 2012;7(4):e33509. doi: 10.1371/journal.pone.0033509. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
22. Wang S, Li R, Yi X, Fang T, Yang J, Bae HJ. Производство изопрена на ферментативном гидролизате скорлупы арахиса с использованием различных методов предварительной обработки. Биомед Рез Инт. 2016;2016. 10.1155/2016/4342892. [Бесплатная статья PMC] [PubMed]
Биомед Рез Инт. 2016;2016. 10.1155/2016/4342892. [Бесплатная статья PMC] [PubMed]
23. Паес Г., Хабрант А., Оссемонд Дж., Чабберт Б. Изучение доступности предварительно обработанных клеточных стенок тополя путем измерения динамики флуоресцентных зондов. Биотехнология Биотопливо. 2017;10(1):15. doi: 10.1186/s13068-017-0704-5. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
24. Mosier N, Wyman C, Dale B, Elander R, Lee Y, Holtzapple M, Ladisch M. Особенности перспективных технологий предварительной обработки лигноцеллюлозной биомассы. Биоресурсная технология. 2005;96(6):673–686. doi: 10.1016/j.biortech.2004.06.025. [PubMed] [CrossRef] [Google Scholar]
25. Чхве И.С., Ви С.Г., Ким С.Б., Бэ Х.Дж. Преобразование отходов кофейного остатка в биоэтанол с использованием предварительной обработки. Биоресурсная технология. 2012; 125:132–137. doi: 10.1016/j.biortech.2012.08.080. [PubMed] [CrossRef] [Google Scholar]
26. Liu ZH, Chen HZ. Производство ксилозы из биомассы кукурузной соломы паровым взрывом в сочетании с ферментативной усвояемостью. Биоресурсная технология. 2015;193:345–356. doi: 10.1016/j.biortech.2015.06.114. [PubMed] [CrossRef] [Академия Google]
Биоресурсная технология. 2015;193:345–356. doi: 10.1016/j.biortech.2015.06.114. [PubMed] [CrossRef] [Академия Google]
27. Тимунг Р., Мохан М., Чилукоти Б., Сасмал С., Банерджи Т., Гоуд В.В. Оптимизация предварительной обработки разбавленной кислотой и горячей водой различной лигноцеллюлозной биомассы: сравнительное исследование. Биомасса Биоэнергия. 2015;81:9–18. doi: 10.1016/j.biombioe.2015.05.006. [CrossRef] [Google Scholar]
28. Васкес М.Дж., Алонсон Дж.Л., Домингес Х., Парахо Дж.К. Получение ксилозосодержащих ферментационных сред путем ферментативного постгидролиза олигомеров, полученных при автогидролизе початков кукурузы. World J Microbiol Biotechnol. 2001;17(8):817–822. doi: 10.1023/A:1013563628882. [Перекрестная ссылка] [Академия Google]
29. Якобсен С.Е., Вайман С.Е. Модели гидролиза целлюлозы и гемицеллюлозы для применения в современных и новых процессах предварительной обработки. Заявл. Биохим Биотехнолог. 2000; 84–86 (1–9): 81–96. doi: 10.1385/ABAB:84–86:1–9:81. [PubMed] [CrossRef] [Google Scholar]
[PubMed] [CrossRef] [Google Scholar]
30. Ализаде Х., Теймури Ф., Гилберт Т.И., Дейл Б.Е. Предварительная обработка проса методом взрыва волокон аммиака (AFEX) Appl Biochem Biotechnol Part A Enzyme Eng Biotechnol. 2005;124(1–3):1133–1141. doi: 10.1385/ABAB:124:1–3:1133. [PubMed] [CrossRef] [Академия Google]
31. Kim S, Holtzapple MT. Кинетика делигнификации кукурузной соломы при предварительной обработке известью. Биоресурсная технология. 2006;97(5):778–785. doi: 10.1016/j.biortech.2005.04.002. [PubMed] [CrossRef] [Google Scholar]
32. Kootstra AMJ, Beeftink HH, Scott EL, Sanders JP. Сравнение предварительной обработки разбавленной минеральной и органической кислотой для ферментативного гидролиза пшеничной соломы. Biochem Eng J. 2009;46(2):126–131. doi: 10.1016/j.bej.2009.04.020. [CrossRef] [Google Scholar]
33. Rabelo SC, Andrade RR, Maciel Filho R, Costa AC. Предварительная обработка щелочной перекисью водорода, ферментативный гидролиз и ферментация жома сахарного тростника до этанола. Топливо. 2014;136:349–357. doi: 10.1016/j.fuel.2014.07.033. [CrossRef] [Google Scholar]
Топливо. 2014;136:349–357. doi: 10.1016/j.fuel.2014.07.033. [CrossRef] [Google Scholar]
34. Jönsson LJ, Alriksson B, Nilvebrant N-O. Биоконверсия лигноцеллюлозы: ингибиторы и детоксикация. Биотехнология Биотопливо. 2013;6(1):16. дои: 10.1186/1754-6834-6-16. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
35. Наир Р.Б., Лундин М., Брандберг Т., Леннартссон П.Р., Тахерзаде М.Дж. Предварительная обработка пшеничных отрубей разбавленной фосфорной кислотой для ферментативного гидролиза и последующего производства этанола съедобными грибами Нейроспора промежуточная . Ind Crops Prod. 2015;69:314–323. doi: 10.1016/j.indcrop.2015.02.038. [CrossRef] [Google Scholar]
36. Kim JS, Lee Y, Kim TH. Обзор технологии щелочной предварительной обработки для биоконверсии лигноцеллюлозной биомассы. Биоресурсная технология. 2016;199:42–48. doi: 10.1016/j.biortech.2015.08.085. [PubMed] [CrossRef] [Google Scholar]
37. da Costa Correia JA, Júnior JEM, Goncalves LRB, Rocha MVP. Предварительная обработка яблочного жмыха кешью щелочной перекисью водорода для производства этанола: исследование параметров. Биоресурсная технология. 2013;139: 249–256. doi: 10.1016/j.biortech.2013.03.153. [PubMed] [CrossRef] [Google Scholar]
Предварительная обработка яблочного жмыха кешью щелочной перекисью водорода для производства этанола: исследование параметров. Биоресурсная технология. 2013;139: 249–256. doi: 10.1016/j.biortech.2013.03.153. [PubMed] [CrossRef] [Google Scholar]
38. Kumar R, Mago G, Balan V, Wyman CE. Физические и химические характеристики твердых частиц кукурузной соломы и тополя, полученные в результате передовых технологий предварительной обработки. Биоресурсная технология. 2009;100(17):3948–3962. doi: 10.1016/j.biortech.2009.01.075. [PubMed] [CrossRef] [Google Scholar]
39. Qiu J, Ma L, Shen F, Yang G, Zhang Y, Deng S, Zhang J, Zeng Y, Hu Y. Предварительная обработка пшеничной соломы фосфорной кислотой с перекисью водорода для ферментативного осахаривания и производства этанола при высокой загрузке твердых веществ. Биоресурсная технология. 2017; 238:174–181. doi: 10.1016/j.biortech.2017.04.040. [PubMed] [CrossRef] [Академия Google]
40. Qiu J, Wang Q, Shen F, Yang G, Zhang Y, Deng S, Zhang J, Zeng Y, Song C. Оптимизация предварительной обработки пшеничной соломы фосфорной кислотой и перекисью водорода (PHP) методом поверхности отклика для ферментативных осахаривание. Заявл. Биохим Биотехнолог. 2017;181(3):1123–1139. doi: 10.1007/s12010-016-2273-7. [PubMed] [CrossRef] [Google Scholar]
Оптимизация предварительной обработки пшеничной соломы фосфорной кислотой и перекисью водорода (PHP) методом поверхности отклика для ферментативных осахаривание. Заявл. Биохим Биотехнолог. 2017;181(3):1123–1139. doi: 10.1007/s12010-016-2273-7. [PubMed] [CrossRef] [Google Scholar]
41. Sun RC, Fang J, Tomkinson J. Делигнификация ржаной соломы с использованием перекиси водорода. Ind Crops Prod. 2000;12(2):71–83. дои: 10.1016/S0926-6690(00)00039-Х. [CrossRef] [Google Scholar]
42. Li M, Foster C, Kelkar S, Pu Y, Holmes D, Ragauskas A, Saffron CM, Hodge DB. Структурная характеристика трав, предварительно обработанных щелочной перекисью водорода, демонстрирующих различные фенотипы лигнина. Биотехнология Биотопливо. 2012;5(1):38. дои: 10.1186/1754-6834-5-38. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
43. Chen J-H, Xu J-W, Shing C-X. Скорость разложения отбеливающих агентов перекиси водорода в различных химических и физических условиях. Джей Простет Дент. 1993;69(1):46–48. doi: 10.1016/0022-3913(93)-K. [PubMed] [CrossRef] [Google Scholar]
1993;69(1):46–48. doi: 10.1016/0022-3913(93)-K. [PubMed] [CrossRef] [Google Scholar]
44. Xiang Q, Lee Y. Окислительный крекинг осажденного лигнина лиственных пород перекисью водорода. Заявл. Биохим Биотехнолог. 2000;84(1):153–162. doi: 10.1385/ABAB:84–86:1–9:153. [PubMed] [CrossRef] [Google Scholar]
45. Gellerstedt G, Agnemo R. Реакции лигнина с щелочной перекисью водорода. Часть 3. Окисление сопряженных карбонильных структур. Acta Chem Scand B. 1980; 34:4. [Академия Google]
46. Чжан С., Ту М., Пейс М.Г. Пути к потенциальным биопродуктам из лигноцеллюлозной биомассы, лигнина и гемицеллюлозы. БиоЭнерджи Рез. 2011;4(4):246–257. doi: 10.1007/s12155-011-9147-1. [CrossRef] [Google Scholar]
47. Li C, Knierim B, Manisseri C, Arora R, Scheller HV, Auer M, Vogel KP, Simmons BA, Singh S. Сравнение предварительной обработки проса разбавленной кислотой и ионной жидкостью: биомасса сопротивляемость, делигнификация и ферментативное осахаривание. Биоресурсная технология. 2010;101(13):4900–4906. doi: 10.1016/j.biortech.2009.10.066. [PubMed] [CrossRef] [Google Scholar]
2010;101(13):4900–4906. doi: 10.1016/j.biortech.2009.10.066. [PubMed] [CrossRef] [Google Scholar]
48. Shuai L, Amiri MT, Questell-Santiago YM, Héroguel F, Li Y, Kim H, Meilan R, Chapple C, Ralph J, Luterbacher JS. Стабилизация формальдегидом способствует образованию мономера лигнина в процессе деполимеризации биомассы. Наука. 2016;354(6310):329–333. doi: 10.1126/science.aaf7810. [PubMed] [CrossRef] [Google Scholar]
49. Gil A, Neto CP. Исследования твердого ЯМР древесины и других лигноцеллюлозных материалов. Annu Rep ЯМР Spectrosc. 1999;37:75–117. doi: 10.1016/S0066-4103(08)60014-9. [CrossRef] [Google Scholar]
50. Wi SG, Cho EJ, Lee DS, Lee SJ, Lee YJ, Bae HJ. Преобразование лигноцеллюлозы в биотопливо: новая предварительная обработка значительно улучшает последующий биокаталитический гидролиз различных лигноцеллюлозных материалов. Биотехнология Биотопливо. 2015;8(1):228. doi: 10.1186/s13068-015-0419-4. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
51. Матулова М., Нуай Р., Чапек П., Пеан М., Форано Э., Делорт А-М. Деградация пшеничной соломы на Fibrobacter succinogenes S85: исследование ядерного магнитного резонанса в жидком и твердом состоянии. Appl Environ Microbiol. 2005;71(3):1247–1253. doi: 10.1128/AEM.71.3.1247-1253.2005. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Матулова М., Нуай Р., Чапек П., Пеан М., Форано Э., Делорт А-М. Деградация пшеничной соломы на Fibrobacter succinogenes S85: исследование ядерного магнитного резонанса в жидком и твердом состоянии. Appl Environ Microbiol. 2005;71(3):1247–1253. doi: 10.1128/AEM.71.3.1247-1253.2005. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
52. Karimi K, Taherzadeh MJ. Критический обзор аналитических методов предварительной обработки лигноцеллюлозы: состав, визуализация и кристалличность. Биоресурсная технология. 2016; 200:1008–1018. doi: 10.1016/j.biortech.2015.11.022. [PubMed] [CrossRef] [Академия Google]
53. Wei S, Kumar V, Banker G. Опосредованная фосфорной кислотой деполимеризация и декристаллизация целлюлозы: получение низкокристаллической целлюлозы — нового фармацевтического эксципиента. Инт Дж Фарм. 1996;142(2):175–181. doi: 10.1016/0378-5173(96)04673-X. [CrossRef] [Google Scholar]
54. Qin Y, Wei X, Liu X, Wang T, Qu Y. Очистка и характеристика рекомбинантной эндоглюканазы Trichoderma reesei, экспрессированной в Saccharomyces cerevisiae с более высоким гликозилированием и стабильностью. Protein Expr Purif. 2008;58(1):162–167. doi: 10.1016/j.pep.2007.09.004. [PubMed] [CrossRef] [Google Scholar]
Protein Expr Purif. 2008;58(1):162–167. doi: 10.1016/j.pep.2007.09.004. [PubMed] [CrossRef] [Google Scholar]
55. Karlsson J, Siika-aho M, Tenkanen M, Tjerneld F. Ферментативные свойства низкомолекулярных эндоглюканаз Cel12A (EG III) и Cel45A (EG V) Trichoderma ризей . Дж Биотехнолог. 2002;99(1):63–78. doi: 10.1016/S0168-1656(02)00156-6. [PubMed] [CrossRef] [Google Scholar]
56. Penttilä M, Lehtovaara P, Nevalainen H, Bhikhabhai R, Knowles J. Гомология между генами целлюлазы Trichoderma reesei : полная нуклеотидная последовательность гена эндоглюканазы I. Ген. 1986;45(3):253. doi: 10.1016/0378-1119(86)
-5. [PubMed] [CrossRef] [Google Scholar]57. Tomme P, Tilbeurgh H, Pettersson G, Damme J, Vandekerckhove J, Knowles J, Teeri T, Claeyssens M. Исследования целлюлозолитической системы Trichoderma reesei QM 9414 FEBS J. 1988;170(3):575–581. [PubMed] [Google Scholar]
58. Миллс Т.Ю., Сандовал Н.Р., Гилл Р.Т. Токсичность гидролизата целлюлозы и механизмы толерантности у Escherichia coli . Биотехнология Биотопливо. 2009 г.;2(1):26. doi: 10.1186/1754-6834-2-26. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Биотехнология Биотопливо. 2009 г.;2(1):26. doi: 10.1186/1754-6834-2-26. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
59. Palmqvist E, Hahn-Hägerdal B. Ферментация лигноцеллюлозных гидролизатов. II: ингибиторы и механизмы торможения. Биоресурсная технология. 2000;74(1):25–33. doi: 10.1016/S0960-8524(99)00161-3. [CrossRef] [Google Scholar]
60. Zaldivar J, Ingram LO. Влияние органических кислот на рост и ферментацию этанологенной Escherichia coli LY01. Биотехнология Биоинж. 1999;66(4):203–210. doi: 10.1002/(SICI)1097-0290(1999)66:4<203::AID-BIT1>3.0.CO;2-#. [PubMed] [CrossRef] [Google Scholar]
61. Zaldivar J, Martinez A, Ingram LO. Влияние выбранных альдегидов на рост и ферментацию этанологенной Escherichia coli . Биотехнология Биоинж. 1999;65(1):24–33. doi: 10.1002/(SICI)1097-0290(19991005)65:1<24::AID-BIT4>3.0.CO;2-2. [PubMed] [CrossRef] [Google Scholar]
62. Olofsson K, Bertilsson M, Lidén G. Краткий обзор SSF — интересного варианта процесса производства этанола из лигноцеллюлозного сырья. Биотехнология Биотопливо. 2008;1(1):7. дои: 10.1186/1754-6834-1-7. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
Биотехнология Биотопливо. 2008;1(1):7. дои: 10.1186/1754-6834-1-7. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
63. Kim HM, Wi SG, Jung S, Song Y, Bae HJ. Эффективный подход к производству биоэтанола из красных водорослей Gelidium amansii . Биоресурсная технология. 2015; 175:128–134. doi: 10.1016/j.biortech.2014.10.050. [PubMed] [CrossRef] [Google Scholar]
64. Sluiter A, Hames B, Ruiz R, Scarlata C, Sluiter J, Templeton D, Crocker D. Определение структурных углеводов и лигнина в биомассе. Лабораторный анальный процесс. 2008; 1617:1–16. [Google Scholar]
65. Вуд ТМ, Бхат КМ. Методы измерения активности целлюлазы. Методы Энзимол. 1988;160:87–112. doi: 10.1016/0076-6879(88)60109-1. [CrossRef] [Google Scholar]
66. Bae HJ, Kim HJ, Kim YS. Производство рекомбинантной ксиланазы в растениях и ее потенциал для биоотбеливания целлюлозы. Биоресурсная технология. 2008;99(9):3513–3519. doi: 10.1016/j.biortech.2007.07.064. [PubMed] [CrossRef] [Google Scholar]
67. Чой И.С., Ким Дж.Х., Ви С.Г., Ким К.Х., Бэ Х.Дж. Производство биоэтанола из отходов кожуры мандарина ( Citrus unshiu ) с использованием предварительной обработки. Приложение Энергия. 2013;102:204–210. doi: 10.1016/j.apenergy.2012.03.066. [Перекрестная ссылка] [Академия Google]
Чой И.С., Ким Дж.Х., Ви С.Г., Ким К.Х., Бэ Х.Дж. Производство биоэтанола из отходов кожуры мандарина ( Citrus unshiu ) с использованием предварительной обработки. Приложение Энергия. 2013;102:204–210. doi: 10.1016/j.apenergy.2012.03.066. [Перекрестная ссылка] [Академия Google]
68. Миллер Г.Л. Использование реагента динитросалициловой кислоты для определения редуцирующих сахаров. Анальная хим. 1959; 31 (3): 426–428. doi: 10.1021/ac60147a030. [CrossRef] [Google Scholar]
Морское производство и потребление изопрена в смешанном слое поверхностного океана – полевое исследование в двух океанических регионах
Статьи | Том 15, выпуск 2
Биогеонауки, 15, 649–667, 2018
https://doi.org/10.5194/bg-15-649-2018
© Автор(ы) 2018. Работа распространяется под номером
Лицензия Creative Commons Attribution 4.0.
Исследовательская статья 01 фев 2018
Исследовательская статья | 01 фев 2018
Деннис Буге 1 , Кэтлин Шлундт 2 , Астрид Брахер 3,4 , Соня Эндрес 1 , Бирте Цэнкер 1 и Криста А. Марандино 2 6
Деннис Буге и др.
Деннис Буге 1 ,Cathleen Schlundt 2 ,Astrid Bracher 3,4 ,Sonja Endres 1 ,Birthe Zäncker 1 ,and Christa A. Marandino 2
Марандино 2 6
Деннис Буге и др.
Деннис Буге 1 ,Cathleen Schlundt 2 ,Astrid Bracher 3,4 ,Sonja Endres 1 ,Birthe Zäncker 1 ,and Christa A. Marandino 2
Show author details
- 1 GEOMAR Центр океанических исследований имени Гельмгольца, Киль, Германия
- 2 Морская биологическая лаборатория, MBL, Вудс-Хоул, Массачусетс, США
- 3 Институт Альфреда Вегенера – Центр полярных и Морские исследования, Бремерхафен, Германия
- 4 Институт физики окружающей среды Бременского университета, Германия
Получено: 21 июня 2017 г. – Начало обсуждения: 29 июня 2017 г. – Пересмотрено: 24 ноября 2017 г. – Принято: 9 декабря 2017 г. – Опубликовано: 1 февраля 2018 г.
Аннотация. Параметризации концентраций изопрена на поверхности океана многочисленны, несмотря на отсутствие понимания процесса источника/поглотителя. Здесь мы представляем изопрен и связанные с ним полевые измерения в смешанном слое из Индийского океана и восточной части Тихого океана, чтобы исследовать скорость производства и потребления в двух контрастных регионах, а именно в олиготрофном открытом океане и в прибрежной области апвеллинга. Наши данные показывают, что способность различных функциональных типов фитопланктона (PFT) производить изопрен, по-видимому, в основном зависит от света, температуры океана и солености. Наши полевые измерения также показывают, что наличие питательных веществ, по-видимому, оказывает прямое влияние на производство изопрена. С помощью данных о пигментах мы рассчитываем скорость производства изопрена в полевых условиях для различных PFT при различных биогеохимических и физических условиях. Используя эти новые расчетные объемы производства, мы демонстрируем, что для объяснения измеренной концентрации изопрена необходимы дополнительные значительные и переменные потери, помимо известных химических потерь и потерь из-за газообмена воздух-море.
Здесь мы представляем изопрен и связанные с ним полевые измерения в смешанном слое из Индийского океана и восточной части Тихого океана, чтобы исследовать скорость производства и потребления в двух контрастных регионах, а именно в олиготрофном открытом океане и в прибрежной области апвеллинга. Наши данные показывают, что способность различных функциональных типов фитопланктона (PFT) производить изопрен, по-видимому, в основном зависит от света, температуры океана и солености. Наши полевые измерения также показывают, что наличие питательных веществ, по-видимому, оказывает прямое влияние на производство изопрена. С помощью данных о пигментах мы рассчитываем скорость производства изопрена в полевых условиях для различных PFT при различных биогеохимических и физических условиях. Используя эти новые расчетные объемы производства, мы демонстрируем, что для объяснения измеренной концентрации изопрена необходимы дополнительные значительные и переменные потери, помимо известных химических потерь и потерь из-за газообмена воздух-море.